L'Agència Europea de Medicaments comença a revisar la vacuna francesa Valneva
És el desè vaccí contra la covid-19 que examina el regulador europeu
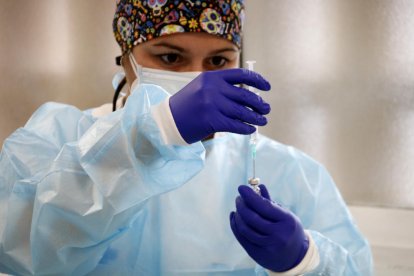
RUTI Immune aconsegueix 1,6 MEUR per desenvolupar una vacuna contra la covid-19
L'Agència Europea de Medicaments (EMA, per les seves sigles en anglès) ha començat a estudiar els resultats preliminars i els estudis clínics inicials en adults de la vacuna contra la covid-19 desenvolupada per Valneva. Com ja ha fet amb altres vaccins contra la covid-19, l'EMA ha iniciat la revisió perquè els estudis «suggereixen que la vacuna provoca la producció d'anticossos i de cèl·lules immunes» contra el virus. La vacuna de Valneva és el desè vaccí que revisa l'EMA. Un cop el regulador europeu tingui suficients evidències de tots els assajos, la companyia podrà demanar formalment l'autorització per comercialitzar la vacuna. Llavors, l'EMA acabarà la revisió de tots els resultats i decidirà si en permet l'ús.
Fins al moment, l'EMA ha autoritzat quatre vacunes: Pfizer-BioNTech, Moderna, AstraZeneca i Janssen. N'hi ha quatre més que continuen el procés de revisió: Novavax, Sputnik, Sinovac i Sanofi Pasteur. Ara s'hi sumarà la de Valneva. A l'octubre, el regulador de la UE va aturar l'examen de la vacuna de CureVac, que va abandonar el desenvolupament de l'antídot pels mals resultats dels assajos clínics.
